ATTENTION : Respectez les minuscules/majuscules. N'oubliez pas les accents !!! Et pas de faute d'orthographe...
Notre Univers évolue depuis sa naissance il y a
d'années (depuis le big-bang) :
- L'Univers est en
.

- Un
de vie et de mort d’étoiles a lieu dans les galaxies.

Notre Univers aujourd’hui contiendrait environ
de galaxies et chaque galaxie contiendrait environ
d’étoiles !
Il y aurait donc 10 000 milliards de milliards d'étoiles dans l'Univers (et surement autant de
qui gravitent autour de cette multitude d'étoiles!).

La matière présente dans l’Univers est constituée d’
, fabriqués pendant le cycle de vie et de mort des étoiles, exceptés les atomes d'hydrogène (
) qui ont été créés 380 000 ans après le big-bang.
Effectivement, pendant sa vie, une étoile (massive) va fabriquer des atomes légers comme l'hélium (He) à partir d'atomes d'hydrogène, puis quand le réservoir d'hydrogène sera épuisé, des atomes plus lourds seront créés comme le carbone (
), l'azote (
), l'oxygène (
) jusqu'au fer (
). Lors de sa mort, l'explosion de l'étoile en supernova (comme Cassiopée A ci-dessous) va donner naissance à des atomes encore plus lourds comme le
(Si), l'or (Au) et l'uranium (U).

Au total,
types d’atomes différents seront formés et puis répandus dans l'espace. On les retrouve tous sur Terre (24 dans le corps humain)... Nous sommes tous des
d'étoiles !
Les atomes ont la propriété de se lier entre eux pour former des
comme l’eau (H
2O), l’ADN (« molécule de la vie »),…


Un atome est constitué d'un
et d'
qui tournent autour.

Le noyau atomique est constitué de
(du latin nucleus, noyau) : des
(de charge positive) + des
(sans charge, électriquement neutres).
Les électrons ont une charge
.
Un atome est électriquement neutre car il possède
de charges positives que de charges négatives. Par conséquent il
chargé électriquement (sa charge totale est nulle).
Le numéro atomique d'un atome dans la classification périodique des éléments (voir ci-dessous) correspond au nombre de
dans le noyau de cet atome.

Par exemple, l'atome ci-dessous est un atome de
et son numéro atomique est égal à
.

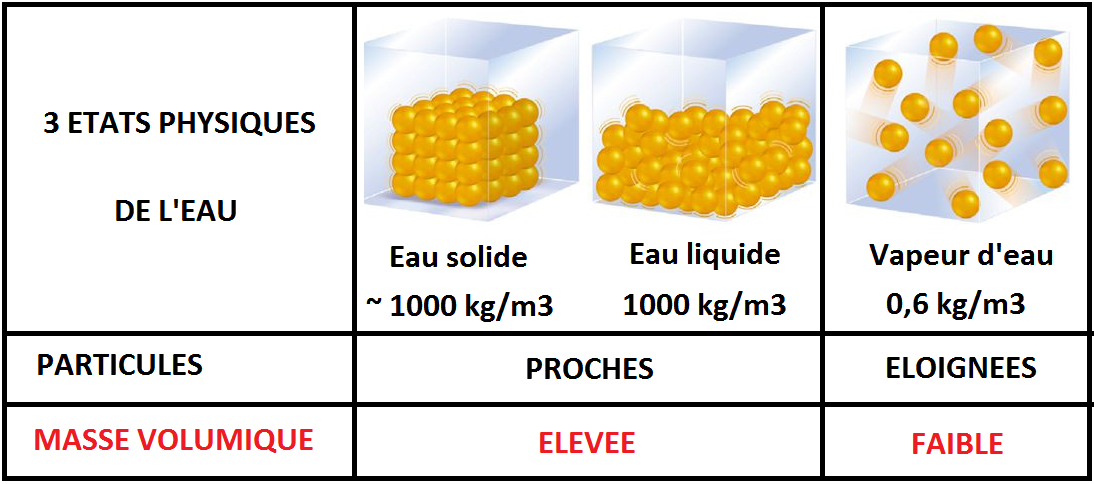
Selon l'
entre les particules de la matière (atomes, molécules), la masse volumique de cette matière est plus ou moins grande, comme pour l'eau ci-dessous :
Pour calculer la masse volumique ρ (« rhô ») d'une substance on utilise la formule :
ρ = m
V où m est la masse de la substance occupant un volume V.
Unité : kilogramme/mètre-cube (kg/m
3) ou gramme/millilitre (
).

Les planètes telluriques (dans l'ordre en s'éloignant du Soleil :
,
,
,
) sont composées essentiellement de
(Fe) et de silicates : roches à base de silice (SiO
2). Leur masse volumique est relativement
(4 000 - 6 000 kg/m
3).
Les planètes géantes (
,
,
,
) sont composées de gaz :
(H
2) + hélium (He) ainsi que de glaces (H
2O,…) de
(Fe) et de silicates. Leur masse volumique est plus
que celle des planètes telluriques (1 000 - 2 000 kg/m
3) car elles contiennent une grande quantité de
.