ATTENTION : Respecter les minuscules/majuscules ! N'oubliez pas les accents ! Pas de faute d'orthographe...

Un atome est une particule
et incassable. Il existe 92 types d'atomes naturels sur Terre. Ils ont été fabriqués dans les
et lors de leur
(supernova).
L'atome d'Hydrogène a pour symbole
et se modélise par une sphère de couleur
.
L'atome de Carbone a pour symbole
et se modélise par une sphère de couleur
.
L'atome d'Oxygène a pour symbole
et se modélise par une sphère de couleur
.
L'atome d'Azote a pour symbole
(
en anglais) et se modélise par une sphère de couleur
.
Une molécule (comme l'ADN ci-dessus) est une particule constituée de plusieurs atomes
entre eux. (Analogie : les mots sont constitués de lettres liées entre elles)
Règles pour écrire la formule d'une molécule :
- On écrit le symbole de chaque type d’atome (dans l’ordre
s’il y en a plusieurs).
- On écrit en indice le nombre d’atomes de chaque type.
Exemples à connaître:
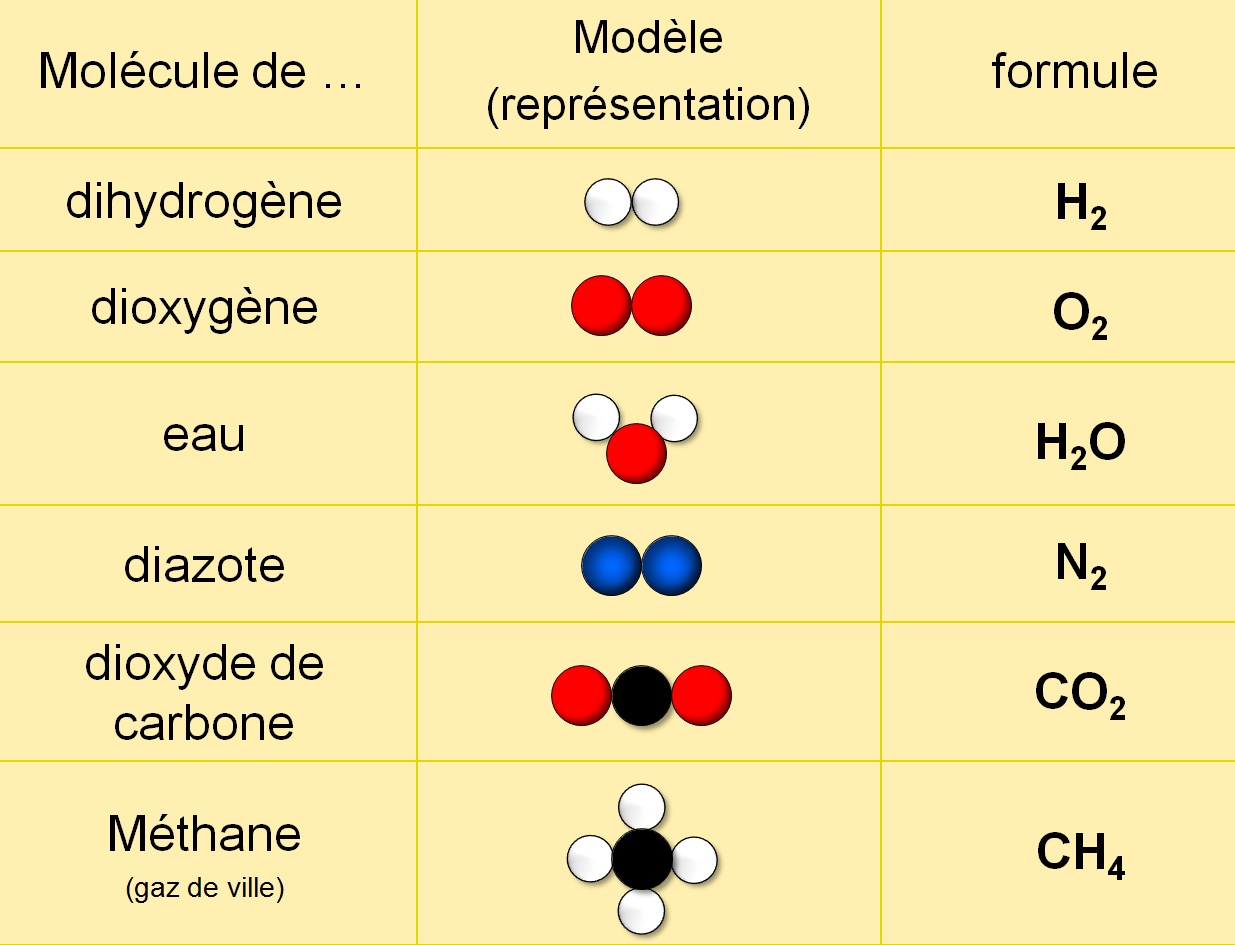
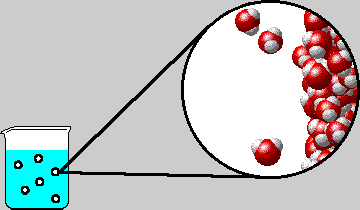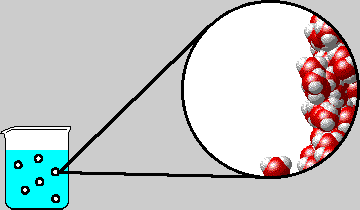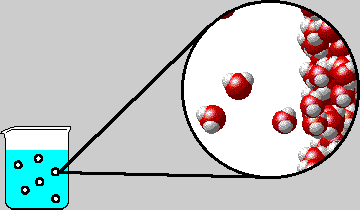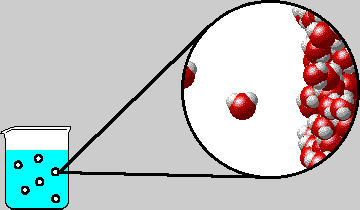
Lors d'une transformation
, les particules restent les mêmes. Seule la distance entre les particules change. Exemples : changements d'état, dissolution, ...
Lors d'une transformation
, les particules elles-mêmes se transforment.
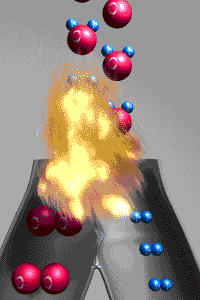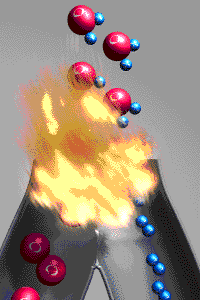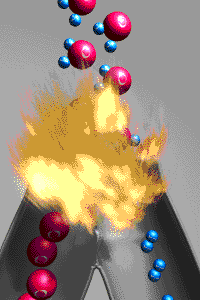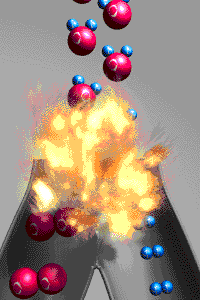
Exemples : caramélisation, respiration, photosynthèse, combustions (comme celle du dihydrogène dans le moteur de fusée ci-dessus),...
Les particules de départ, nommées les
, disparaissent, elles se transforment en
(nouvelles particules formées lors de la transformation).
Lors d’une transformation chimique, les atomes présents dans les réactifs
pour former les produits de la réaction.
Lors d'une transformation physique ou chimique, la masse
car le nombre d'atomes
.
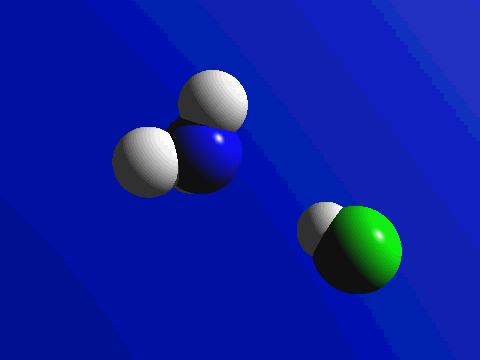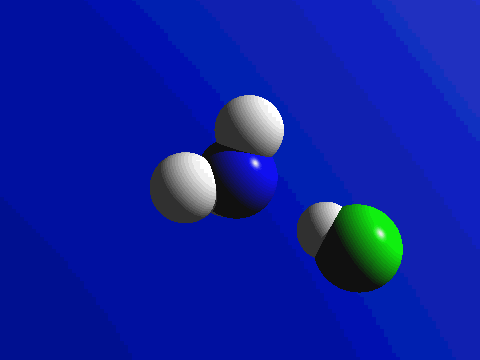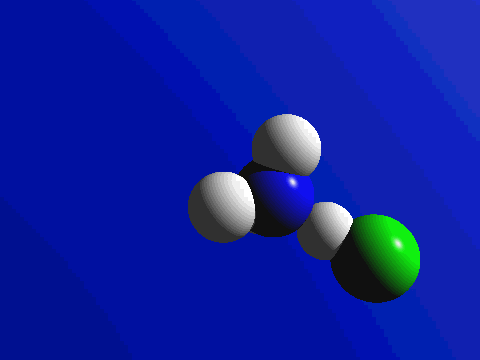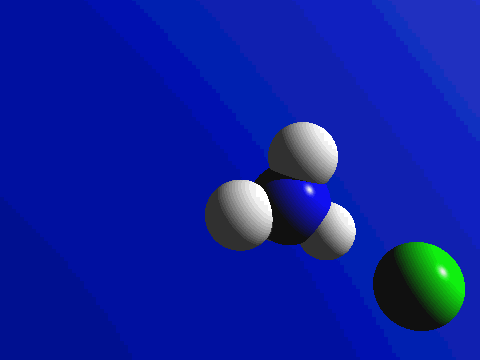
Combustion du méthane (gaz de ville) :
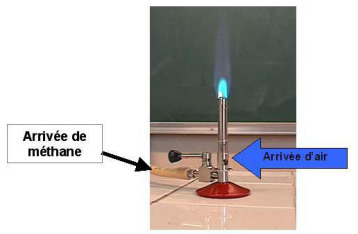
Lors de la combustion complète du méthane :
Les réactifs sont : le
et le
(indispensable à la vie)
Les produits sont : le
(il trouble l'
) et l'
(elle bleuit le sulfate de cuivre anhydre)
Bilan (avec les noms) :
+
-->
+
Equation-bilan (ajuster les coefficients pour équilibrer l'équation, écrire 1 lorsqu'une molécule réagit ou est produite, même si ce n'est pas nécessaire habituellement)
CH
4 +
O
2 --->
CO
2 +
H
2O


Attention : Les combustions peuvent présenter des dangers. Elles peuvent produire un gaz mortel : le monoxyde de carbone (formule :
). C'est le cas lorsque la combustion a lieu avec un manque de dioxygène (on dit que la combustion est incomplète - flamme de gauche de la photo ci-dessus). Veillez donc à ne pas boucher les aérations (qui font entrer du
) et à faire vérifier régulièrement les appareils qui font brûler du gaz.